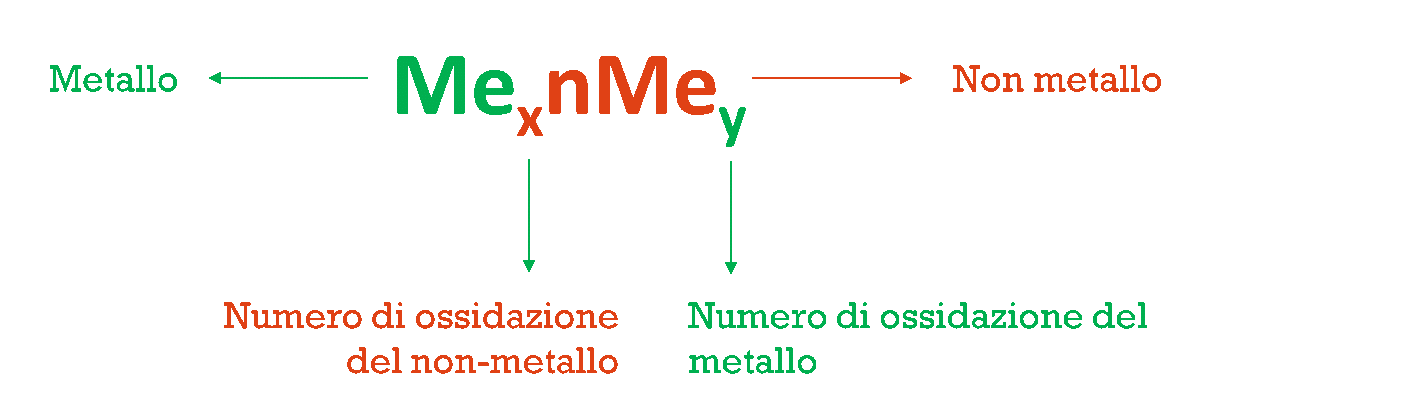
Dopo aver affrontato la parte relativa allo studio della Biologia e aver parlato nello specifico delle proteine, oggi concentriamo l’attenzione su un argomento ostico della chimica per il test di Medicina: la nomenclatura dei composti organici e inorganici.
Cercheremo di semplificare alcuni concetti e darvi dei punti fermi da cui partire per lo studio.
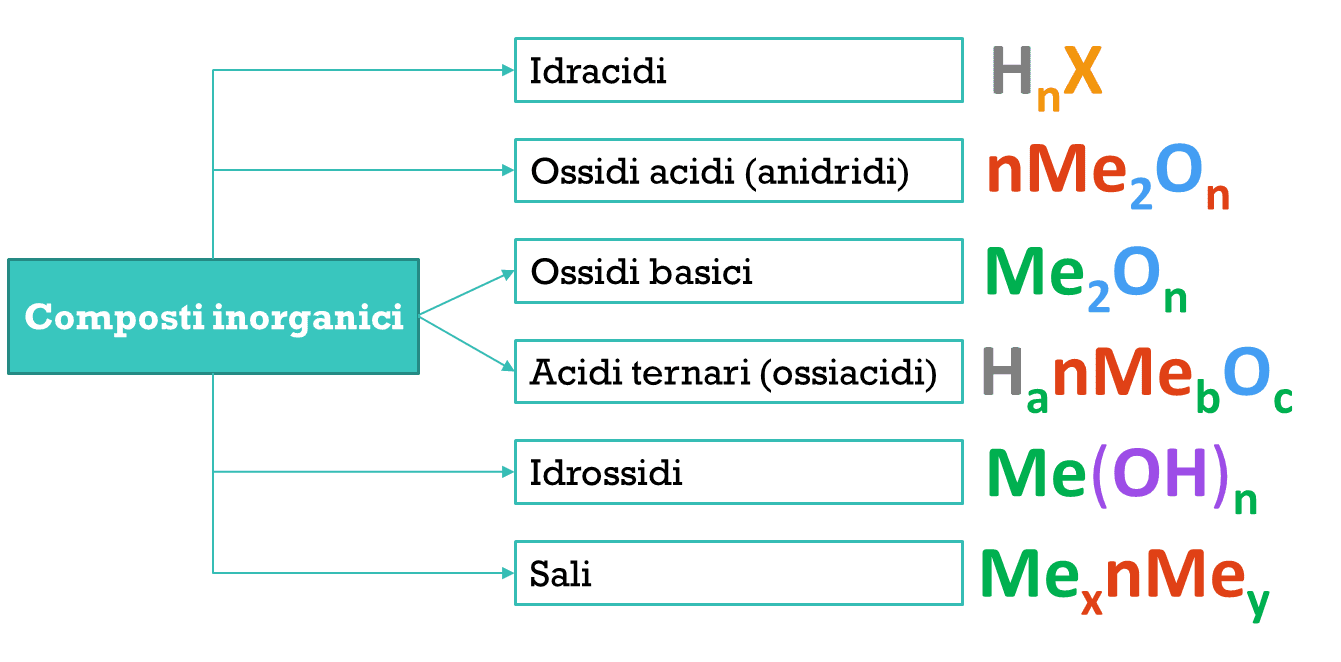
Di questi:
- Idracidi, anidridi e ossidi basici sono composti binari (composti da due elementi chimici diversi)
- Ossiacidi e idrossidi sono composti ternari (composti da tre elementi chimici diversi)
- I Sali possono essere binari o ternari
Table of Contents
Chimica test Medicina: gli idracidi
Gli idracidi ono dei composti binari.
Non viaggiano su rotaia, ma sono costituiti da due soli elementi: l’atomo di idrogeno (che sta un po’ dappertutto, come il prezzemolo) e un alogeno, cioè un elemento del VII gruppo (andate a dare uno sguardo sulla tavola periodica), oppure l’idrogeno e lo zolfo (S).
La formula generica di un idracido quindi sarà quindi “HX”:

Secondo la nomenclatura tradizionale il nome inizia sempre con “acido” (perché questi composti in una soluzione acquosa si comportano da acidi) e si aggiunge il suffisso “-idrico”.

Secondo la nomenclatura IUPAC, invece, si usa il suffisso -uro per l’alogeno, seguito dalla dicitura “di idrogeno”. Vediamo qualche esempio:
Le anidridi
Anche le anidridi sono dei composti binari, ma costituiti da un non metallo e dall’ossigeno.
Il nome deriva dal greco e significa “senza acqua” e possono anche essere chiamati “ossidi acidi”.
La formula generica sarà quindi nMe2On

Secondo la nomenclatura tradizionale, il nome inizia con il termine “anidride”. Qui le cose si complicano un pochino, perché i non-metalli possono formare più anidridi, con aumento del numero di ossidazione e del numero di atomi di ossigeno:
- Se il non-metallo ha un solo numero di ossidazione (come il boro, B) l’anidride è una sola e il suffisso è –ica
- Se il non-metallo ha due numeri di ossidazione (come l’azoto, N) può formare due anidridi con l’ossigeno, e queste avranno i suffissi –osa (quello con il numero di ossidazione minore) e –ica (con il numero di ossidazione maggiore)
- Se il non-metallo ha 4 numeri di ossidazione (solo il cloro, Cl), può formare 4 anidridi diverse con l’ossigeno e si aggiungono anche i prefissi –ipo e –per secondo l’ordine del numero atomico:

Secondo la nomenclatura IUPAC, invece, il nome inizia con il termine “ossido” e si utilizzano i prefissi di-, tri-, tetra-, penta-, esa-, epta- per specificare il numero degli atomi di ciascun elemento. Vediamo qualche esempio:
Gli ossidi basici
Anche gli ossidi basici sono composti binari, “parenti” delle anidridi.
Infatti sono costituiti dall’ossigeno e da un metallo. La formula generica sarà quindi Me2On

Secondo la nomenclatura tradizionale, il nome inizia con il termine “ossidodi”, seguito dal nome del metallo. Se il metallo presenta due numeri di ossidazione, può formare due ossidi diversi con l’ossigeno e in questo caso si utilizzano gli stessi suffissi che abbiamo visto prima, cioè -ico (quello con il numero di ossidazione maggiore) e -oso (quello con il numero di ossidazione minore).

Secondo la nomenclatura IUPAC il nome inizia sempre con “ossido di” e si utilizzano gli stessi prefissi di-, tri-, tetra-, penta-, esa-, epta- per specificare il numero degli atomi di ciascun elemento. Inoltre esiste una terza nomenclatura, chiamata “notazione di Stock” in cui i numeri di ossidazione del metallo vengono distinti con un numero romano (I, II, III, ecc.) tra parentesi alla fine del nome. Vediamo alcuni esempi:
Gli idrossidi
Gli idrossidi sono composti ternari e non binari, perché contengono un ossidrile o gruppo idrossido (-OH)preceduto da un metallo.
Si formano sommando una o più molecole d’acqua ad un ossido. La formula generica, quindi, sarà M(OH)n, quindi un atomo di metallo e tanti gruppi idrossido quanti sono i suoi numeri di ossidazione.

Secondo la nomenclatura tradizionale, il nome inizia con il termine “idrossidodi”, seguito dal nome del metallo. Se il metallo presenta due numeri di ossidazione, può formare due idrossidi diversi con l’ossigeno e in questo caso si utilizzano gli stessi suffissi che abbiamo visto prima, cioè -ico (quello con il numero di ossidazione maggiore) e -oso (quello con il numero di ossidazione minore).

Secondo la nomenclatura IUPAC si utilizzano i prefissidi–, tri–, tetra-, penta-, esa-, per specificare il numero dei gruppi idrossido −OH.

Secondo la notazione di Stock si specificano i numeri di ossidazione con i numeri romani, come nel caso degli ossidi basici. Vediamo alcuni esempi:
Gli ossiacidi o acidi ternari
Gli ossiacidi sono composti ternari, costituiti da idrogeno, ossigeno e un non-metallo, che si formano aggiungendo una o più molecole d’acqua ad un’anidride. La formula chimica generica è HanMebOc

Gli indici a, b, c sono numeri interi primi tra loro, i cui valori corrispondono al numero di atomi di ciascun elemento presenti nei reagenti.

Secondo la nomenclatura tradizionale, il nome si ottiene da quello dell’anidride corrispondente, sostituendo il termine “acido” al termine “anidride”.

Secondo la nomenclatura IUPAC si utilizza sempre la desinenza -ico, preceduta da prefissi per indicare il numero di atomi di ossigeno (osso) e del non metallo e seguita dal numero di ossidazione del non metallo in numeri romani tra parentesi. Quindi: Acido + prefisso numerico + osso + numero di atomi del non-metallo + -ico + (numero di ossidazione del non-metallo). Vediamo alcuni esempi:
I Sali
I Sali sono composti derivanti da un acido per sostituzione degli atomi di idrogeno con un metallo, quindi sono costituiti da un metallo (sotto forma di catione) e da un non-metallo (il residuo di un idracido o di un ossiacido, che funge da anione del sale). Il simbolo del metallo precede quello del non-metallo, perché avendo minore elettronegatività, ha un numero di ossidazione positivo.
A seconda che derivino da ossiacidi o idracidi, prenderanno il nome di Sali ternari (ossiacidi) o binari (idracidi). La formula generale è MexnMey

Secondo la nomenclatura tradizionale:
- Per i Sali binari:
- Se il metallo ha un unico numero di ossidazione il sale prende il nome dal non-metallo terminante nel suffisso -uro, seguito dal nome del metallo
- Se il metallo ha due numeri di ossidazione, nel sale a numero di ossidazione maggiore il metallo prenderà il suffisso -ico, in quello a numero di ossidazione minore prenderà il suffisso -oso
- Per i Sali ternari, i nomi dei residui degli acidi si formano da quelli degli acidi corrispondenti cambiando le desinenze secondo questo schema:
- Oso → ito
- Ico → ato

Secondo la nomenclatura IUPAC:
- Per i Sali binari, il composto prende il nome del non-metallo con la desinenza -uro, seguito dal nome del metallo + i prefissi numerici (di-, tri-, ecc.)
- Per i Sali ternari, si usa la desinenza -ato, i prefissi moltiplicativi per indicare il numero di atomi di ossigeno (osso) e di eventuali altri gruppi e si termina con lo stato di ossidazione del non metallo in numeri romani fra parentesi.
Vediamo infine alcuni esempi:

Come prepararsi
Per una preparazione completa al test di Medicina è disponibile il nuovo Kit EdiTEST composto da:
- Manuale di teoria
- Volume di esercizi e verifiche
- Raccolta di quiz
In omaggio con il kit:
- manuale in versione e-book interattiva
- software di simulazione
- atlante di anatomia virtuale
- video-lezioni online
- e-book “Prove ufficiali 2002-2021”
Simulazione Test Medicina
Vuoi metterti alla prova con le domande generalmente somministrate nei test di Medicina?
Prova la demo gratuita del simulatore EdiTEST>>